Proprietà fisiche e chimiche dello zolfo
Zolfo - abbastanza comune in naturaun elemento chimico (il sedicesimo contenuto nella crosta terrestre e il sesto nelle acque naturali). Esistono sia lo zolfo nativo (stato libero dell'elemento) che i suoi composti.

Zolfo in natura
Tra i più importanti minerali naturali di zolfo,nome pirite di ferro, sfalerite, galena, cinabro, antimonite. Negli oceani, è principalmente contenuto nella forma di solfati di calcio, magnesio e sodio, che determinano la rigidità delle acque naturali.
Come ottengono lo zolfo?
L'estrazione di minerali solforici viene effettuata con metodi diversi. Il modo principale per produrre zolfo è di annusarlo direttamente nel terreno.
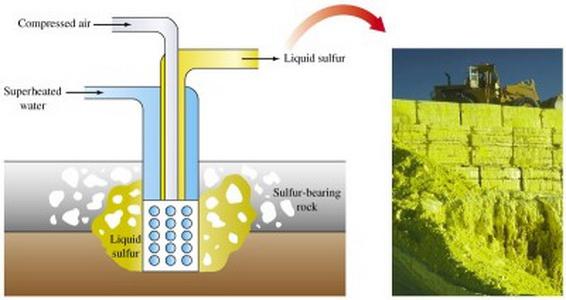
Il metodo di estrazione aperto prevedeL'uso di escavatori, la rimozione di strati di roccia che coprono il minerale sulfurico. Dopo aver frantumato strati di minerale, le esplosioni vengono inviate allo smelter.
Nell'industria, lo zolfo è ricevuto come sottoprodottoprocessi di prodotto in forni per la fusione, durante la raffinazione del petrolio. In grandi quantità, è presente nel gas naturale (sotto forma di anidride solforosa o solfuro di idrogeno), durante l'estrazione di cui è depositato sulle pareti dell'apparecchiatura utilizzata. Lo zolfo a dispersione fine che è stato catturato dal gas è utilizzato nell'industria chimica come materia prima per la produzione di vari prodotti.
Questa sostanza può essere ottenuta da naturalegas di anidride solforosa. Per questo, viene utilizzato il metodo Claus. Consiste nell'applicazione di "pozzi di zolfo" in cui degasifica di zolfo. Il risultato è uno zolfo modificato, ampiamente utilizzato nella produzione di asfalto.
Modifiche di base dello zolfo allotropico
Lo zolfo è inerente all'allotropia. È noto un gran numero di modifiche allotropiche. I più famosi sono lo zolfo rombico (cristallino), monoclino (acicolare) e plastico. Le prime due modifiche sono stabili, la terza alla solidificazione si trasforma in una rombica.

Proprietà fisiche che caratterizzano lo zolfo
Le molecole di modifiche ortorombiche (α-S) e monocliniche (β-S) contengono 8 atomi di zolfo, che sono collegati in un ciclo chiuso da singoli legami covalenti.

In condizioni normali, lo zolfo ha una modificazione rombica. È una sostanza cristallina solida gialla con una densità di 2,07 g / cm3. Si scioglie a 113 ° C. La densità dello zolfo monoclino è di 1,96 g / cm3, il suo punto di fusione è di 119,3 ° C.
Quando si scioglie, lo zolfo aumenta di volume ediventa un liquido giallo che si rompe a una temperatura di 160 ° C e si trasforma in una massa viscosa marrone scuro quando raggiunge circa 190 ° C. A temperature superiori a questo valore, la viscosità dello zolfo diminuisce. A circa 300 ° C, si trasforma nuovamente in uno stato fluido scorrevole. Ciò è spiegato dal fatto che durante il processo di riscaldamento, lo zolfo viene polimerizzato, aumentando la lunghezza della catena con l'aumentare della temperatura. E quando il valore della temperatura supera i 190 ° C, le unità polimeriche vengono distrutte.

Quando lo scioglimento dello zolfo viene raffreddato in modo naturaleun crogiolo cilindrico formato un cosiddetto grumo zolfo - cristalli rombici di grandi dimensioni, di forma distorta di ottaedri con parte "tagliare" bordi o angoli.
Se la sostanza fusa è sottoposta a un forteraffreddamento (ad esempio, con l'aiuto di acqua fredda), è possibile ottenere zolfo plastico, che è una massa elastica gommosa di colore marrone o rosso scuro con una densità di 2,046 g / cm3. Questa modifica, a differenza del rombo emonoclino, è instabile. Gradualmente (entro poche ore) cambia colore in giallo, diventa fragile e si trasforma in rombico.
Quando si congelano i vapori di zolfo (fortemente riscaldati) con azoto liquido, si forma la sua modificazione viola, che è stabile a temperature inferiori a meno 80 ° C.
Nell'ambiente acquoso, lo zolfo è praticamente insolubile. Tuttavia, è caratterizzato da una buona solubilità nei solventi organici. Cattiva condotta elettricità e calore.
Il punto di ebollizione dello zolfo è 444,6 ° C. Il processo di ebollizione è accompagnato dal rilascio di vapori giallo-arancio costituiti prevalentemente dalla S8, che si dissociano al successivo riscaldamento, dando luogo alla formazione di forme di equilibrio di S6, S4 e S2. Inoltre, al riscaldamento, decadono grandi molecole e a temperature superiori a 900 gradi, le coppie consistono essenzialmente di sole molecole S2, dissociando in atomi a 1500 ° C.
Quali sono le proprietà chimiche dello zolfo?
Lo zolfo è un tipico non metallico. È chimicamente attivo. ossidazione-Le proprietà riducenti dello zolfo si manifestano inrelazione al set di elementi. Quando è riscaldato, è facilmente collegato a praticamente tutti gli elementi, il che spiega la sua presenza obbligatoria nei minerali metallici. Le eccezioni sono Pt, Au, I2, N2 e gas inerti. Grado di ossidazione, che mostra lo zolfo nei composti, -2, +4, +6.
Le proprietà dello zolfo e dell'ossigeno causano la sua combustione nell'aria. Il risultato di questa interazione è la formazione di zolfo (SO2) e solforico (SO3) anidridi utilizzati per la produzione di acido solforico e solforico.
A temperatura ambiente, le proprietà riducenti dello zolfo si manifestano solo rispetto al fluoro, nella reazione con cui si forma esafluoruro di zolfo:
- S + 3F2 = SF6.
Quando riscaldato (sotto forma di fusione) interagisce con cloro, fosforo, silicio, carbonio. Come conseguenza delle reazioni con l'idrogeno, oltre all'idrogeno solforato, forma solfati combinati con la formula generale H2SH.
Quando si osservano proprietà ossidanti dello zolfointerazione con metalli. In alcuni casi, si possono osservare reazioni abbastanza violente. Come risultato dell'interazione con i metalli, si formano solfuri (composti di zolfo) e polisolfuri (metalli a multi-zolfo).
Con riscaldamento prolungato, reagisce con agenti ossidanti acidi concentrati, mentre si ossida.
Successivamente, consideriamo le principali proprietà dei composti dello zolfo.
Anidride solforosa
Ossido di zolfo (IV), chiamato anche biossido di zolfoe anidride solforosa, è un gas (incolore) con un forte odore asfissiante. Ha la proprietà di essere liquefatto sotto pressione a temperatura ambiente. SO2 è un ossido acido. Caratterizzato da buona solubilità in acqua. Questo produce un acido solforoso debole, instabile, che esiste solo in soluzione acquosa. Come risultato dell'interazione di anidride solforosa con alcali, si formano solfiti.
Differisce piuttosto alta chimicaattività. Le più pronunciate sono le proprietà chimiche riducenti dell'ossido di zolfo (IV). Tali reazioni sono accompagnate da un aumento del grado di ossidazione dello zolfo.
Le proprietà chimiche ossidative dell'ossido di zolfo si manifestano in presenza di forti agenti riducenti (ad esempio, monossido di carbonio).
Triossido di zolfo
Il triossido di zolfo (anidride solforosa) è l'ossido più altozolfo (VI). In condizioni normali, è un liquido incolore e volatile con un odore soffocante. Ha la proprietà di congelamento a temperature inferiori a 16,9 gradi. Si forma una miscela di diverse modifiche cristalline del triossido di zolfo solido. Elevate proprietà igroscopiche dell'ossido di zolfo lo inducono a "fumare" nell'aria umida. Di conseguenza, si formano goccioline di acido solforico.
Acido solfidrico
L'idrogeno solforato è un composto chimico binario di idrogeno e zolfo. H2S è un gas tossico, incolore, caratteristicole cui caratteristiche sono il sapore dolciastro e l'odore delle uova marce. Si scioglie a meno 86 ° С, bolle a meno 60 ° С. È termicamente instabile. A valori di temperatura superiori a 400 ° C, l'idrogeno solforato si decompone in S e H2. È caratterizzato da buona solubilità in etanolo. Si dissolve male in acqua. Come risultato della dissoluzione in acqua, si forma un acido solfidrico debole. L'idrogeno solforato è un forte agente riducente.

Infiammabile. Quando brucia nell'aria, puoi vedere una fiamma blu. In alte concentrazioni è in grado di reagire con molti metalli.
Acido solforico
Acido solforico (H2SO4) può essere di diversa concentrazione e purezza. In stato anidro è un liquido oleoso incolore che non ha odore.
La temperatura alla quale la sostanzasi scioglie, è 10 ° C. Il punto di ebollizione è 296 ° C. Si dissolve bene in acqua. Quando si scioglie l'acido solforico, si formano gli idrati e viene rilasciata una grande quantità di calore. Il punto di ebollizione di tutte le soluzioni acquose alla pressione di 760 mm Hg. Art. supera i 100 ° С. Il punto di ebollizione aumenta con l'aumentare della concentrazione di acido.

Le proprietà acide della sostanza si manifestano interagendo con ossidi e basi basici. H2SO4 è un acido dibasico, in conseguenza del quale può formare sia solfati (sali medi) che idrogenensolfati (sali acidi), la maggior parte dei quali sono solubili in acqua.
Le proprietà più pronunciate dell'acido solforico si manifestano nelle reazioni di riduzione dell'ossidazione. Questo perché nella composizione di H2SO4 lo zolfo ha uno stato di ossidazione più elevato (+6). Come esempio della manifestazione delle proprietà ossidanti dell'acido solforico, possiamo citare la reazione con il rame:
- Cu + 2H2SO4 = CuSO4 + 2H2O + SO2.
Zolfo: proprietà utili
Lo zolfo è un microelemento necessario perorganismi viventi. È parte integrante degli amminoacidi (metionina e cisteina), enzimi e vitamine. Questo elemento prende parte alla formazione della struttura terziaria della proteina. La quantità di zolfo legato chimicamente contenuto nelle proteine è su una base di peso da 0,8 a 2,4%. Il contenuto dell'elemento nel corpo umano è di circa 2 grammi per 1 kg di peso (cioè circa lo 0,2% è di zolfo).
Proprietà utili di microelementi difficilisovrastimare Proteggendo il protoplasma del sangue, lo zolfo è un assistente attivo del corpo nella lotta contro i batteri nocivi. La quantità di coagulazione dipende dalla sua quantità, cioè l'elemento aiuta a mantenere il suo livello sufficiente. Inoltre, lo zolfo gioca un ruolo importante nel mantenere le normali concentrazioni di bile prodotta dall'organismo.
È spesso chiamato il "minerale di bellezza", perchéè semplicemente necessario preservare la salute della pelle, delle unghie e dei capelli. Chere è la capacità intrinseca di proteggere un organismo da vari tipi di influenza negativa dell'ambiente. Questo aiuta a rallentare il processo di invecchiamento. Lo zolfo pulisce il corpo dalle tossine e protegge dalle radiazioni, il che è particolarmente vero ora, data l'attuale situazione ambientale.
Una quantità insufficiente di oligoelementi nel corpo può comportare una scarsa escrezione di scorie, ridotta immunità e vitalità.
Lo zolfo è un partecipante alla fotosintesi batterica. È un costituente della batterioclorofilla e l'idrogeno solforato è una fonte di idrogeno.
Zolfo: proprietà e applicazioni nell'industria
Lo zolfo più usato è usato perproduzione di acido solforico. Inoltre, le proprietà di questa sostanza consentono di essere utilizzato per la vulcanizzazione della gomma, come fungicida in agricoltura e anche per un farmaco (zolfo colloidale). Inoltre, lo zolfo è utilizzato per la produzione di fiammiferi e composti pirotecnici, fa parte delle composizioni bituminose di zolfo per la produzione di asfalto di zolfo.
</ p>


